| Ernest Rutherford |
|
| Naissance | 30
Août 1871 à Brightwater (Nouvelle-Zélande)  |
| Décès | 19
Octobre 1937 Cambridge (Royaume Uni)  |
| Domicile | Angleterre |
|
Nationalité |
Néo-zélandais |
| Profession |
Physicien et chimiste |
Peu après la découverte de
la radioactivité, le physicien Rutherford fera deux découvertes d'une
importance capitale dans la recherche de la structure de l'atome. Il
recevra le prix Nobel de chimie en 1908 pour ses recherches sur la
désintégration des éléments et la chimie des substances radioactives.
Introduction aux atomes :
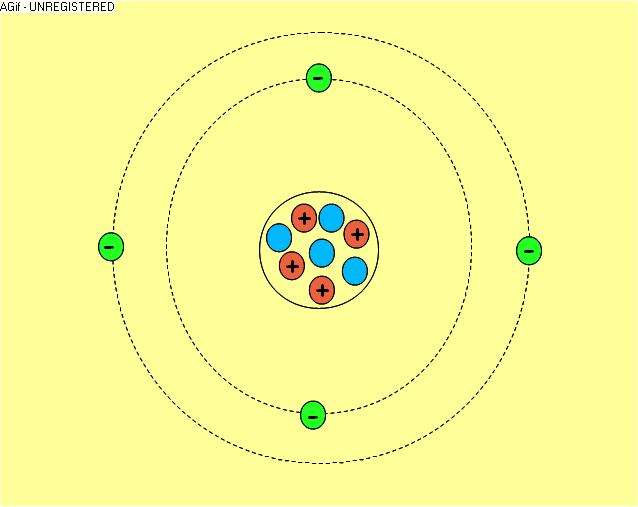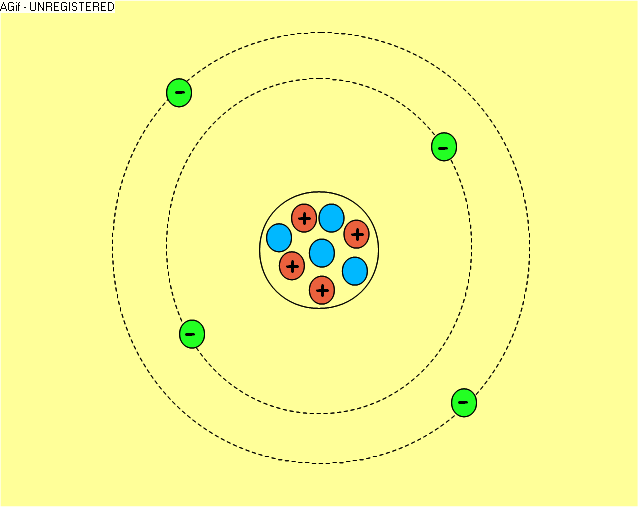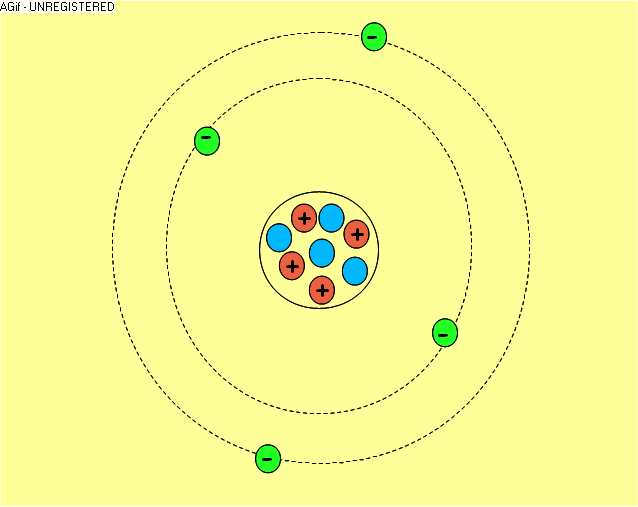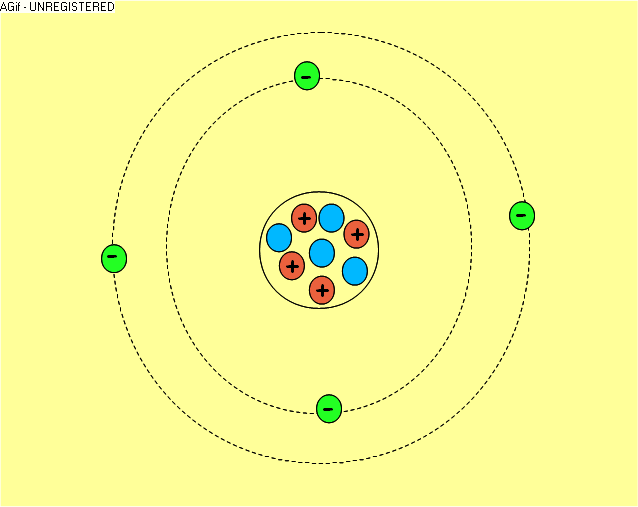
La
matière qui nous entoure est constituée de molécules formées par des
atomes. Les atomes sont formés par un noyau autour duquel gravitent des
électrons chargés négativement. Le noyau est formé de deux types de
particules : les neutrons qui n'ont pas de charge et les protons,
chargés négativement. Lorsque les noyaux des atomes renferment trop
d'énergie, les proton et les neutrons ne se maintiennent plus ensemble.
Alors, les noyaux des atomes finissent par libérer leur trop plein
d'énergie en émettant des rayonnements.
C'est ce phénomène de désintégration que l'on appelle
radioactivité.
Découvertes
:
-
Première découverte : En 1898, il démontre que les substances radioactives émettent deux types de radiations: alpha (a) et bêta (b).
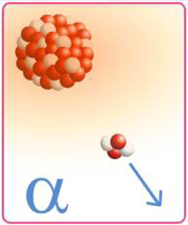 |
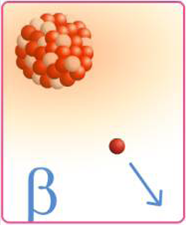 La radioactivité bêta se traduit par la transformation dans le noyau : d'un proton en neutron ou d'un neutron en proton. |
-
Deuxième découverte : En 1907, Thomson demande à son élève Rutherford de vérifier l'exactitude de son modèle atomique. Celui-ci accepte et réalise cette expérience :
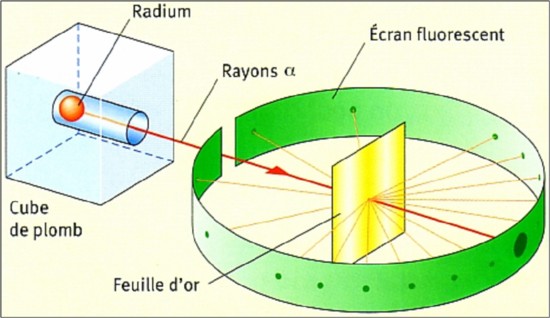
Il remarque que :
-
La plupart des particules alpha traversent les atomes d'or sans être déviées comme si elles n'avaient jamais rencontré les atomes d'or.
-
Plusieurs particules alpha sont légèrement déviées lors de la traversée de la feuille d'or.
-
Certaines particules alpha rebondissent carrément vers la source comme si elles avaient frappé un mur.
En 1911, Rutherford propose son modèle atomique : -
L'atome est constitué principalement de vide
-
Le centre de l'atome, qu'il nomme « noyau » est minuscule et concentre presque toute la masse de l'atome. Le noyau est chargé positivement
-
Les électrons (chargés négativement) tournent autour du noyau à une très grande vitesse
-
L'atome est électriquement neutre : la somme de la charge des électrons est égale à la charge du noyau.
Modèle "planétaire" de Rutherford
Ce modèle sera contesté puis remplacé par le modèle atomique de Bohr, remplacé lui-même par des modèles plus récents et plus complexes.
Dilan SUNAR et Anthony ROPP